
Органические соединения, содержащие альдегидную группу -СН=О, называются альдегидами. Вместе с кетонами они относятся к карбонильным веществам. Общая формула альдегидов и кетонов – CnH2nO или R-CHO.
Виды
Классификация альдегидов по двум признакам приведена в таблице.
|
Признак |
Вид |
Описание |
Пример |
|
Возможность образовывать новые связи |
Предельные |
Содержат максимальное количество атомов водорода |
Ацетальдегид |
|
Непредельные |
Способны присоединять атомы водорода |
Акролеин |
|
|
Ароматические |
Циклические соединения с тремя двойными связями |
Бензальдегид |
|
|
Количество карбонильных групп |
Простые |
Содержат только одну группу =С=О |
Формальдегид |
|
Диальдегиды |
Содержат две группы =С=О |
Глиоксаль |
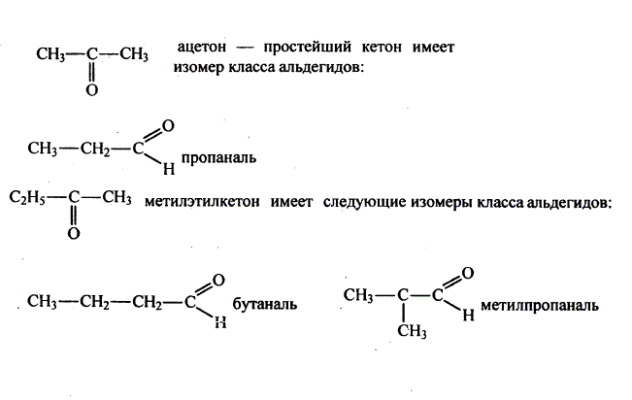
Альдегидам, начиная с бутаналя, характерны два вида изомерии: межклассовая с кетонами и структурная. Например, изомерия углеродного скелета: СН3-СН2-СН2-СН=О (бутаналь) и СН3-СН(СН3)-СН=О (2-метилпентаналь). При присоединении к водороду метиленовой группы СН2 из пропаналя образуется пропанол (ацетон): СН3-СН2-СОН → СН3-СО-СН3.
Получение
Соединения получают:
- окислением спиртов оксидом меди (II):
R-CH2-OH + CuO → R-CHO + Cu + H2O;
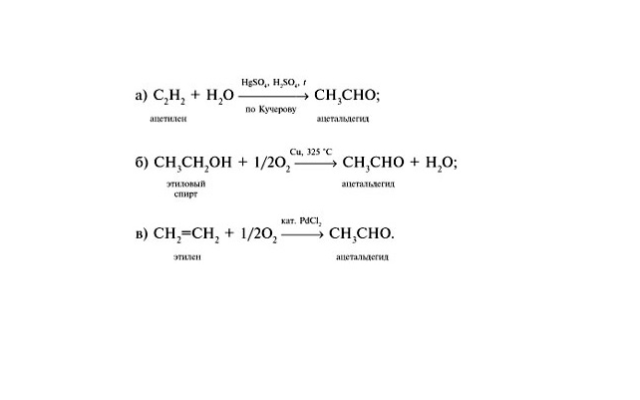
- гидратацией ацетилена (получение ацетальдегид):
H-С≡C-H + H2O → CH3CHO;
- окислением этилена:
2C2H4 + O2 → 2CH3CHO;
- окислением метана (получение формальдегида):
CH4 + O2 → CH2O + H2O;
- дегидрированием спиртов:
CH3-CH(OH)-CH3 → CH3-CO-CH3 + H2.
Физические свойства
Физическое состояние альдегидов зависит от количества атомов углерода:
- формальдегид – газообразное вещество;
- альдегиды, содержащие от двух до 12 атомов углерода, – жидкости;
- альдегиды с 13 и более атомами углерода – твёрдые вещества.
Температуры кипения альдегидов, имеющих линейное строение, выше, чем у разветвлённых изомеров. Плотность, вязкость, показатель преломления при нормальных условиях увеличиваются с возрастанием молекулярной массы.
Два первых альдегида в гомологическом ряду – формальдегид и этаналь – неограниченно смешиваются с водой. Далее в гомологическом ряду растворимость уменьшается с увеличением углеродного скелета. Альдегиды хорошо растворяются в спиртах, эфирах и других органических растворителях.
Гомологи С8-С13 используются в парфюмерной промышленности.
Химические свойства
Функциональная альдегидная группа определяет химические свойства альдегидов, которые аналогичны свойствам кетонов. Ниже описаны основные реакции с альдегидами.
|
Реакция |
Описание |
Уравнение |
|
Присоединения |
Альдегиды присоединяют молекулы воды, спиртов, тиололов, неорганических солей, аминов по двойной связи карбонильной группы |
|
|
Восстановление |
При взаимодействии с водородом образуются спирты |
HCHO + H2 → CH3OH |
|
Окисление |
Качественные реакции оксидом серебра («серебряное зеркало») и гидроксидом меди (II) с образованием красного осадка |
|
Что мы узнали?
Из урока химии 10 класса узнали, что такое альдегиды. Это родственные кетонам вещества, содержащие группу -СН=О. Альдегиды образуют гомологический ряд с общей формулой CnH2nO. Названия в ряду соответствуют названиям алканов с суффиксом «аль». Простейший альдегид – формальдегид или метаналь – бесцветный газ. Альдегиды ряда С2-С12 – жидкости. Высшие альдегиды с 13 и более атомами углерода – твёрдые вещества. Альдегиды участвуют в реакциях окисления, восстановления, присоединения.