
Типичный неметалл – сера – относится к группе халькогенов и находится в VI группе периодической таблицы Менделеева. Сера – один из жизненно важных элементов, входящих в состав живых организмов.
В соединениях проявляет себя как окислитель, отнимая электроны. Однако возможность переходить в возбуждённое состояние за счёт свободных d-орбиталей даёт элементу две дополнительные степени окисления – +4 и +6.
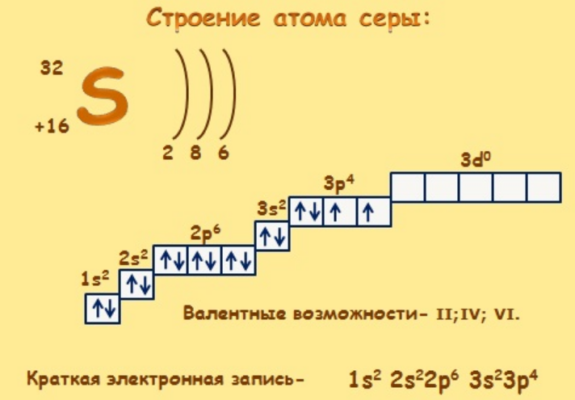
Известно четыре стабильных изотопа серы, находящиеся в природе. Это 32S, 33S, 34S, 36S. Кроме того, искусственно получено 20 радиоактивных изотопов серы.
Аллотропия
Сера – хрупкое кристаллическое вещество желтоватого цвета. При нагревании плавится, превращаясь в жидкость жёлтого цвета. При увеличении температуры до 200°С становится вязкой тёмно-коричневой массой, напоминающей смолу.
Основные физические свойства элемента:
- отсутствие растворимости в воде, в том числе в составе сложных веществ;
- плавучесть в воде (не смачивается);
- плохая проводимость тепла и электричества;
- хорошая растворимость в органических растворителях (феноле, бензоле, сероуглероде);
- диссоциация на атомы происходит при температуре 1500°С;
- температура кипения – 444,6°С.
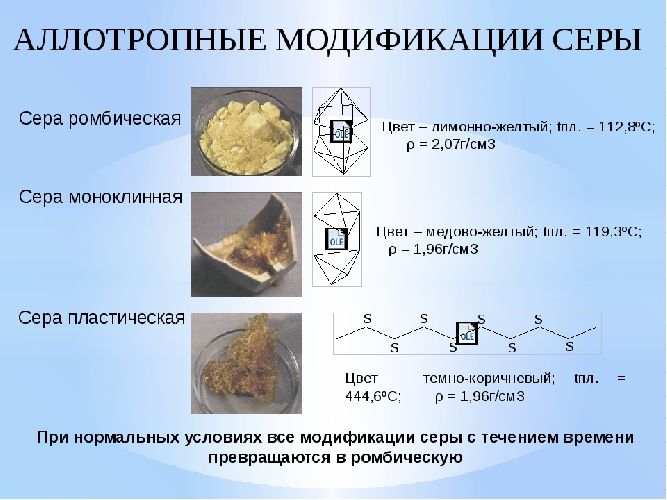
Сера образует аллотропные модификации, которые отличаются физическими свойствами. Краткое описание модификаций приведено в таблице.
|
Вид |
Формула |
Температура плавления, °С |
Плотность, г/см3 |
Особенности |
|
Ромбическая |
S8 |
113 |
2,07 |
Наиболее устойчивая модификация |
|
Моноклинная |
S8 |
119 |
1,96 |
Устойчива при температуре 96°С и более. В обычных условиях превращается в ромбическую |
|
Пластическая |
Sn |
119 |
1,96 |
Коричневая вязкая масса. Полимер. Неустойчива, самопроизвольно превращается в ромбическую |
Свойства
В зависимости от реакции сера проявляет разную степень окисления:
- -2 – в реакциях с металлами и неметаллами (Al2S3, SiS2, Na2S);
- +4 – в реакциях с галогенами и кислородом (SCl4, SBr4, SF4, SO2);
- +6 – в реакциях с элементами, имеющими большую электроотрицательность (H2SO4, SF6, SO3).
Сера – активное вещество, образующее кислоты, соли, оксиды. Общие химические свойства элемента приведены в таблице.
|
Реакция |
Описание |
Уравнение |
|
С металлами |
В обычных условиях реагирует только с активными металлами. С остальными реакция протекает при нагревании. С золотом и платиной не реагирует. Образуются сульфиды |
– 2Na + S → Na2S; – Cu + S → CuS; – Zn + S → ZnS |
|
С неметаллами |
С водородом реагирует при 150-200°С, с кислородом – при 280-360°С. С фосфором и углеродом реагирует в отсутствии воздуха при нагревании. Реакция с фтором протекает в присутствии катализатора |
– H2 + S → H2S; – S + O2 → SO2; – 2S + 3O2 → 2SO3; – 2P + 3S → P2S3; – 2S + C → CS2; – S + 3F2 → SF6 |
|
С кислотами |
Проявляет свойства восстановителя |
S + 2HNO3 → 2NO + H2SO4 |
|
Диспропорционирование |
Реакция со щёлочью образует сульфиды и сульфиты |
3S + 6KOH → K2S+4O3 + 2K2S-2 + 3H2O |
В природе сера находится в составе минералов, горных пород, полезных ископаемых. Например, в составе гипса (CaSO4⋅2H2O), пирита (FeS2), глауберовой соли (Na2SO4⋅10H2O). Серу как продукт метаболизма вырабатывают некоторые бактерии. Сера присутствует в составе белков.

Что мы узнали?
Из урока химии 9 класса узнали об особенностях строения и свойствах серы. Это 16 элемент периодической таблицы, содержащий шесть валентных электронов. Сера проявляет три степени окисления – +4, +6, -2. Элемент образует три модификации – ромбическую, моноклинную, пластическую серу. Реагирует с металлами, неметаллами, кислотами и щелочами. Соли серы с металлами называются сульфидами. Сера входит в состав живых организмов. В природе находится в составе минералов.