
Неметаллы – химические элементы, которые имеют типичные неметаллические свойства и располагаются в правом верхнем углу Периодической системы. Какие же свойства присущи этим элементам, и с чем реагируют неметаллы?

С увеличением заряда ядра атома наблюдается закономерность изменения свойств химических элементов от металлических к неметаллическим.
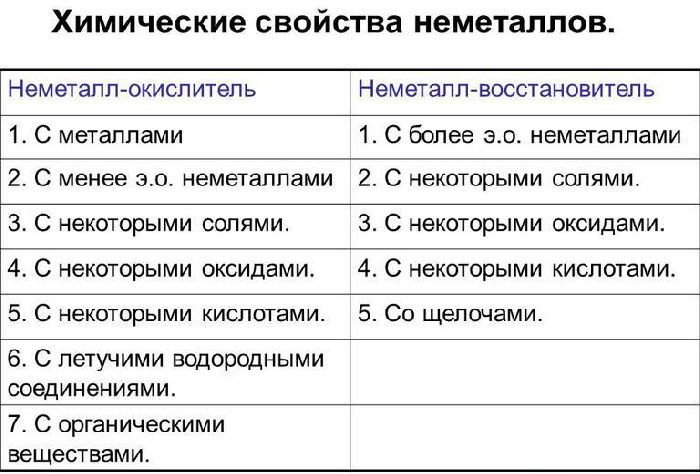
Химические свойства неметаллов
Водородные свойства неметаллов в основном являются летучими соединениями, которые в водных растворах имеют кислотный характер. Они имеют молекулярные структуры, а также ковалентную полярную связь. Некоторые, например, вода, аммиак или фтороводород образуют водородные связи. Соединения образуются при непосредственном взаимодействии неметаллов с водородом. Пример:
Все водородные соединения имеют восстановительные свойства, причем их восстановительная сила возрастает справа налево по периоду и сверху вниз в группе. Так, сероводород сгорает при большом количестве кислорода:
Окисление может идти по другому пути. Так, уже на воздухе водный раствор сероводорода мутнеет в результате образования серы:
Соединения неметаллов с кислородом, как правило, являются кислотными оксидами, которым соответствуют кислородосодержащие кислоты (оксокислоты). Структура оксидов типичных неметаллов молекулярная.
Чем выше степень окисления неметалла, тем сильнее соответствующая кислородосодержащая кислота. Так, хлор непосредственно не взаимодействует с кислородом, однако образует ряд оксокислот, которым соответствуют оксиды, ангидриды этих кислот.
Наиболее известны такие соли этих кислот, как хлорная известь CaOCl2 (смешанная соль хлорноватистой и хлороводородной кислот), бертолетова соль KClO3 (хлорат калия).
Азот в оксидах проявляет положительные степени окисления +1, +2, +3, +4, +5. Первые два оксида N2O и NO – несолеобразующие и являются газами. N2O3 (оксид азота III) – является ангидридом азотистой кислоты HNO2 . Оксид азота IV – бурый газ NO2 – газ, который хорошо растворяется в воде, образуя при этом две кислоты. Этот процесс можно выразить уравнением:

Ангидрид азотной кислоты N2O5 – белое кристаллическое вещество, которое легко растворяется в воде. Пример:
Соли азотной кислоты называются селитрами, они растворимы в воде. Соли калия, кальция, натрия используют для получения азотных удобрений.
Фосфор образует оксиды, проявляя степени окисления +3 и +5. Наиболее устойчивый оксид – фосфорный ангидрид P2O5 , образующий молекулярную решетку, в узлах которой находятся димеры P4O10 . Соли ортофосфорной кислоты применяются в качестве фосфорных удобрений, например, аммофос NH4 H2 PO4 (дигидрофосфат аммония).
Таблица расположения неметаллов
| Группа | I | III | IV | V | VI | VII | VIII |
| Первый период | H | He | |||||
| Второй период | B | C | N | O | F | Ne | |
| Третий период | Si | P | S | Cl | Ar | ||
| Четвертый период | As | Se | Br | Kr | |||
| Пятый период | Te | I | Xe | ||||
| Шестой период | At | Rn |
Что мы узнали?
В школьной программе по химии (8-9 класс) большое внимание уделяется изучению общих свойств неметаллов. В данной статье изучается информация, чем отличаются металлы от неметаллов, и какими особенностями они обладают. Также приведена таблица химических свойств неметалов.