
Класс ациклических непредельных или ненасыщенных углеводородов, содержащих в молекуле две двойные связи, называется алкадиены или диеновые углеводороды. Подробнее о свойствах и характеристиках алкадиенов читайте ниже.
- С3Н4 – пропадиен;
- С4Н6 – бутадиен;
- С5Н8 – пентадиен;
- С6Н10 – гексадиен;
- С7Н12 – гептадиен;
- С8Н14 – октадиен;
- С9Н16 – нонадиен;
- С10Н18 – декадиен.
Физические свойства гомологов ряда пропадиена аналогичны свойствам алкенам. Пропадиен и бутадиен – газы, легко переходящие в жидкое состояние. Гомологи С5-С17 и их изомеры – жидкости. Высшие алкадиены с 18 и более атомами углерода – твёрдые соединения.
Изомерия
Гомологи от пентадиена и выше образуют пространственную и структурную изомерии. Для диенов характерна геометрическая пространственная изомерия. Они образуют цис- и транс-изомеры.
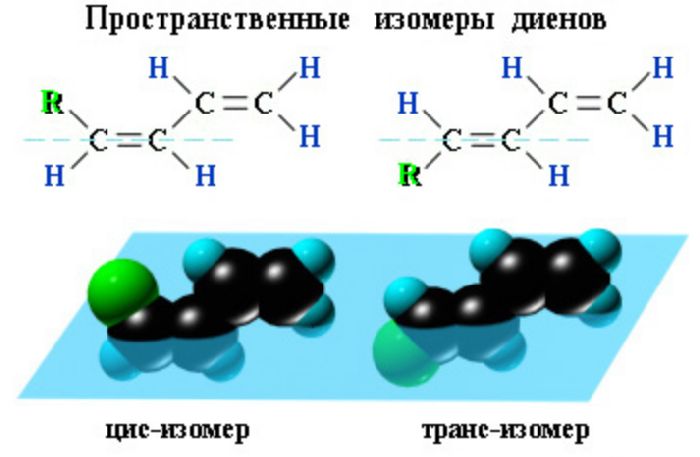
Структурная изомерия осуществляется по углеродному скелету и по положению кратных связей. При переносе метильной группы к другому атому углерода образуются структурные изомеры диенов. Например, 2-метилбутадиен-1,3 или изопрен – изомер пентадиена-1,3 с метильной группой у второго атома углерода.

В зависимости от расположения связей друг к другу выделяют три вида диенов:
- кумулированные – двойные связи находятся у одного атома углерода (СН2=С=СН2);
- сопряжённые – двойные связи разделены одинарной связью (CH2=CH-CH=CH2);
- изолированные – двойные связи разделены неограниченным количеством простых связей (CH2=CH-CH2-CH=CH2).
Диены получают из этанола, нефтепродуктов, галогеналканов.
Свойства
За счёт кратных связей диены могут вступать в реакции присоединения. Атомы присоединяются к месту разрыва связи. При этом в зависимости от положения кратных связей при одних и тех же реакциях образуются вещества с разными структурами. В таблице описаны основные химические реакции диенов.
|
Реакция |
Описание |
Уравнение |
|
Гидрирование |
Присоединение атома водорода в присутствии никеля |
CH2=CH-CH=CH2 + 2H2 → CH3-CH2-CH2-CH3 |
|
Галогенирование |
Образование тетрагалогеноалканов |
CH2=CH-CH=CH2 + Br2 → CH2(Br)-CH(Br)-CH=CH2 или CH2(Br)-CH=CH-CH2-Br |
|
Гидрогалогенирование |
Реакция протекает в жидкой среде (спиртовой или водной) в присутствии катализатора – хлорида лития |
CH2=CH-CH=CH2 +HBr → CH3-CH(Br)-CH=CH2 или CH3-CH=CH-CH2-Br |
|
Полимеризация |
Получение искусственного каучука |
nCH2=CH-CH=CH2 → (-CH2-CH=CH-CH2-)n |
Основное использование алкадиенов – синтез каучука.

Что мы узнали?
Диены или алкадиены – ненасыщенные ациклические углеводороды, содержащие двойные связи. Низшие алкадиены – газы и жидкости, высшие (более 18 атомов углерода) – твёрдые вещества. Простейший представитель класса – пропадиен, образующий гомологический ряд. Для диенов характерна пространственная и структурная изомерии. Структурная изомерия происходит по положению двойных связей и по углеродному скелету. Алкадиены более активны, чем насыщенные углеводороды. Вещества участвуют в реакции присоединения по месту разрыва двойной связи.