
Важнейшим опытом, демонстрирующим сложное строение атома, стал опыт физика Э. Резерфорда. Рассмотрим суть этого опыта.
Экспериментальная установка состояла из контейнера с радием, испускающим α-частицы, на пути частиц ставилась тонкая металлическая фольга, а за фольгой устанавливался экран, покрытый сульфидом цинка, на котором при попадании α-частиц возникало свечение (сцинтилляция). Схема опыта представлена на следующем рисунке:
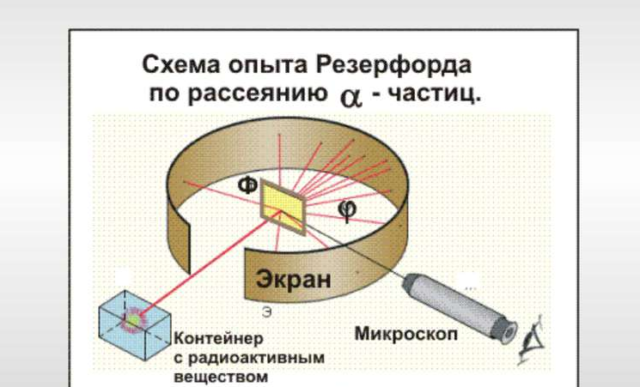
Без фольги, в точке облучения возникало сцинтилляционное пятно. Если на пути полета α-частиц поместить фольгу – размер пятна увеличится за счет рассеяния частиц из-за взаимодействия с положительными зарядами. По характеру изменения пятна можно судить о распределении положительного заряда в атомах вещества.
Результаты опыта
Если положительный заряд равномерно распределен по веществу, рассеяния α-частиц не будет. В соответствии с моделью атома Томсона, положительные заряды имеют некоторую пространственную неоднородность, а значит, рассеяние появится.
Рассеяние, действительно, появилось, но при этом имело довольно интересное распределение – некоторая часть частиц отклонялась на довольно заметные углы, иногда на большие, чем была рассчитана установка.
Это уже говорило о большой неравномерности распределения положительного заряда. Установка была модифицирована, экраны стали устанавливаться вокруг нее.
И с большим удивлением Резерфорд обнаружил, что небольшое число частиц (около 0,05%) отклоняются на очень большие углы, более 90⁰, некоторые – даже «отскакивали» от фольги в обратном направлении.
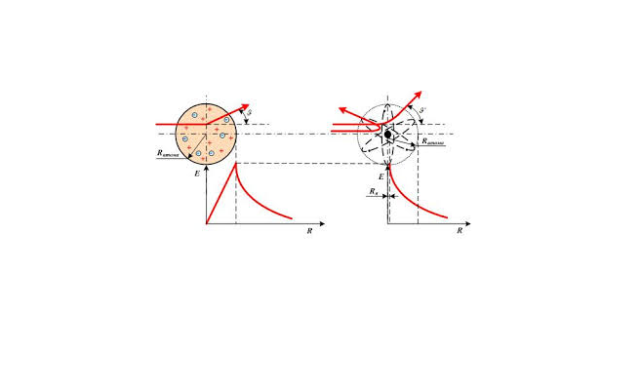
Для такого «отскока» потенциальная энергия электрического отталкивания должна быть равна кинетической энергии α-частицы:
$${q_αqover 4πε_0R}={m_α{v_α}^2over 2}$$
В левой части этой формулы – потенциальная энергия взаимодействия, а в правой – кинетическая энергия частицы.
Если предположить, что положительный заряд имеет радиус порядка $10^{-10}$м, то заряд $q$ должен почти в сто тысяч раз превышать заряд электрона. Поскольку атом нейтрален, то можно предположить, что число электронов в сто тысяч раз больше, чем число атомов. Однако, такое число электронов имеют значительную массу, которая не регистрируется в опыте.
Следовательно, положительный заряд сосредоточен в очень небольшой части атома, которая была названа ядром. Расчеты показали, что размер ядра атома имеет величину порядка $10^{-14}-10^{-15}$м. Электроны же движутся вокруг ядра на большом расстоянии. Была построена планетарная модель атома:
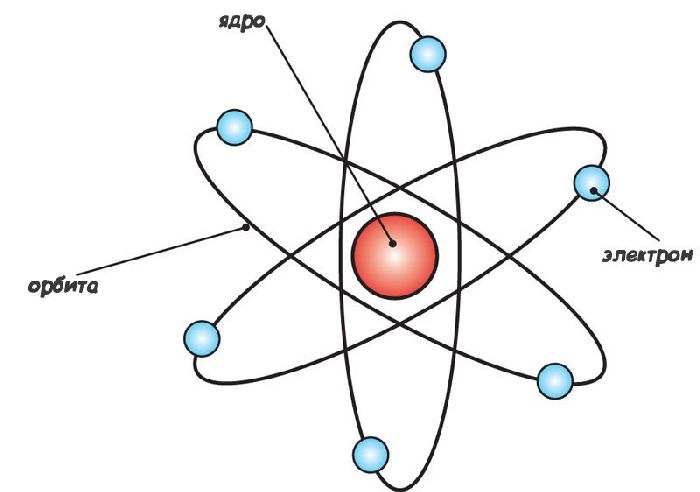
Опыт Резерфорда также позволяет оценить и заряд ядра. Он оказался разным для разных материалов, и если принять за единицу заряд электрона, то заряд ядра оказался равным порядковому номеру элемента в таблице Менделеева.
Если атом увеличить до размеров орбиты Земли, размер ядра окажется в сто раз меньше, чем размер Солнца.
Что мы узнали?
В опыте Э.Резерфорда по рассеянию альфа частиц поток частиц направлялся на тонкую фольгу, после которой на экране можно было видеть картину рассеяния. Оказалось, что некоторые частицы отклоняются на очень большие углы. Это говорило о том, что положительно заряженный заряд внутри атома сосредоточен в очень малой части атома, которая была названа ядром.